価標とは 647927-化学基礎 価標とは
· 最後の段落で、水素原子の価標の数は1としましたが、 正しくは価標の数ではなく原子価となります。 補足になりますが、分子のときは価標といい、原子のときは原子価といいます。カールフィッシャー法とは(1)式のように水と選択的に、かつ定量的に反応するカールフィッシャー試薬 (よう素、二酸化硫黄、塩基、及びアルコール等の溶剤より構成)を用いて水分を測定する方法です。 I 2 +SO 2 +3Base+ROH+H 2 O ⇒ 2Base・HI+Base・HSO 4 R(1) この方法には電量滴定法と容量滴定法があります。 国内ではJIS (日本産業規格)はもちろんJAS (日本 · 2 価標*(英語bondは「結合」の意味で使われる) 提案:特別な呼称をつけない(必要なら「線」「結合」などと呼ぶ)。 3 希ガス*(対応する
分子と共有結合
化学基礎 価標とは
化学基礎 価標とは-常用対数の覚え方 常用対数については以下の3つを覚えれば十分です。 log 10 2 ≒ \log_ {10} 2\fallingdotseq log10 2 ≒ これは「おっさん多い」というのが有名ですが, 0 0 0 が多くて比較的覚えやすいので,自分はそのまま丸覚えしました。力価標定標準試薬 固体水標準試料(検定結果証明書付) 水標準液(検定結果証明書付) プロピレンカーボネート プロピレンカーボネート プロピレンカーボネート 5mLアンプル 10本/ケース 5mLアンプル 10本/ケース 8mLアンプル 10本/ケース 力価 02±001mgH2O/g 力



受験基礎化学 11 共有結合 共有結合結晶 みかみの参考書ブログ
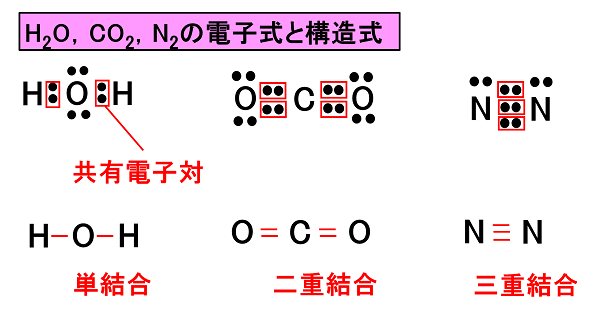
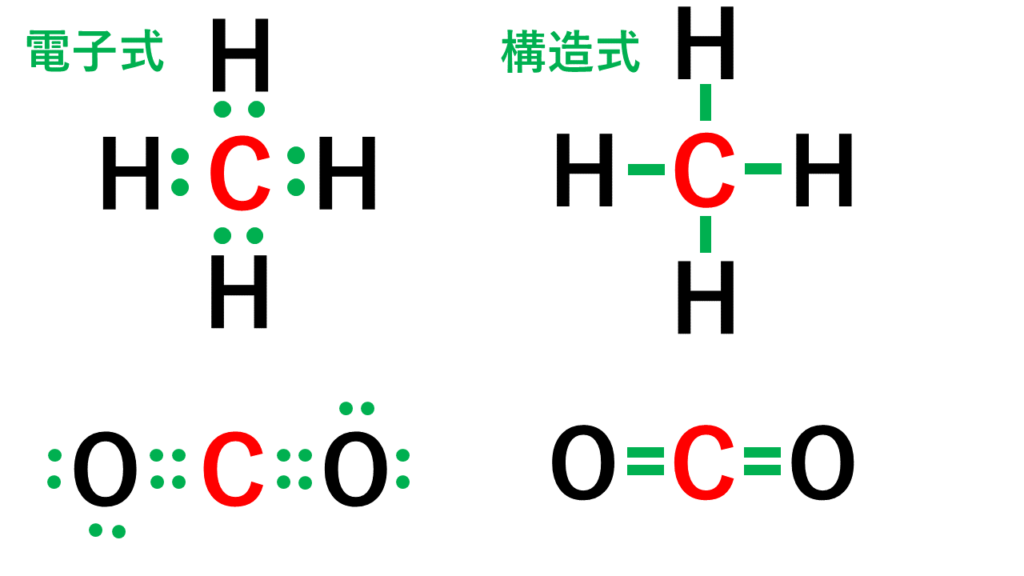
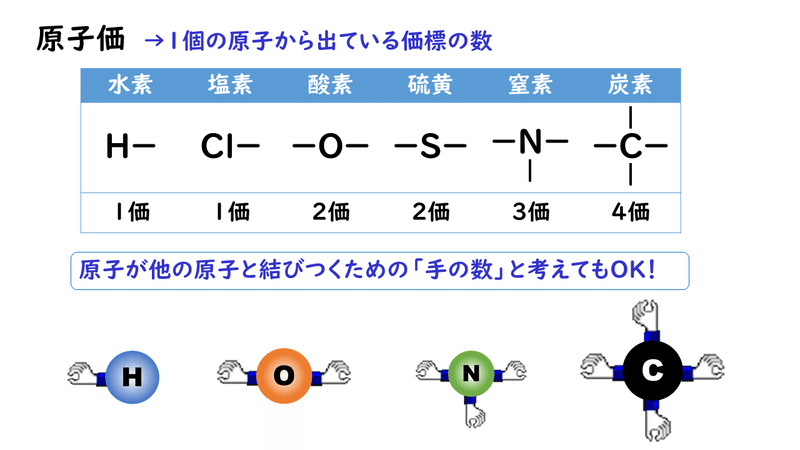
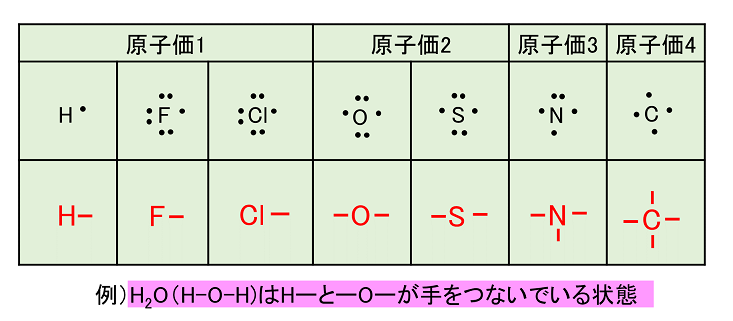
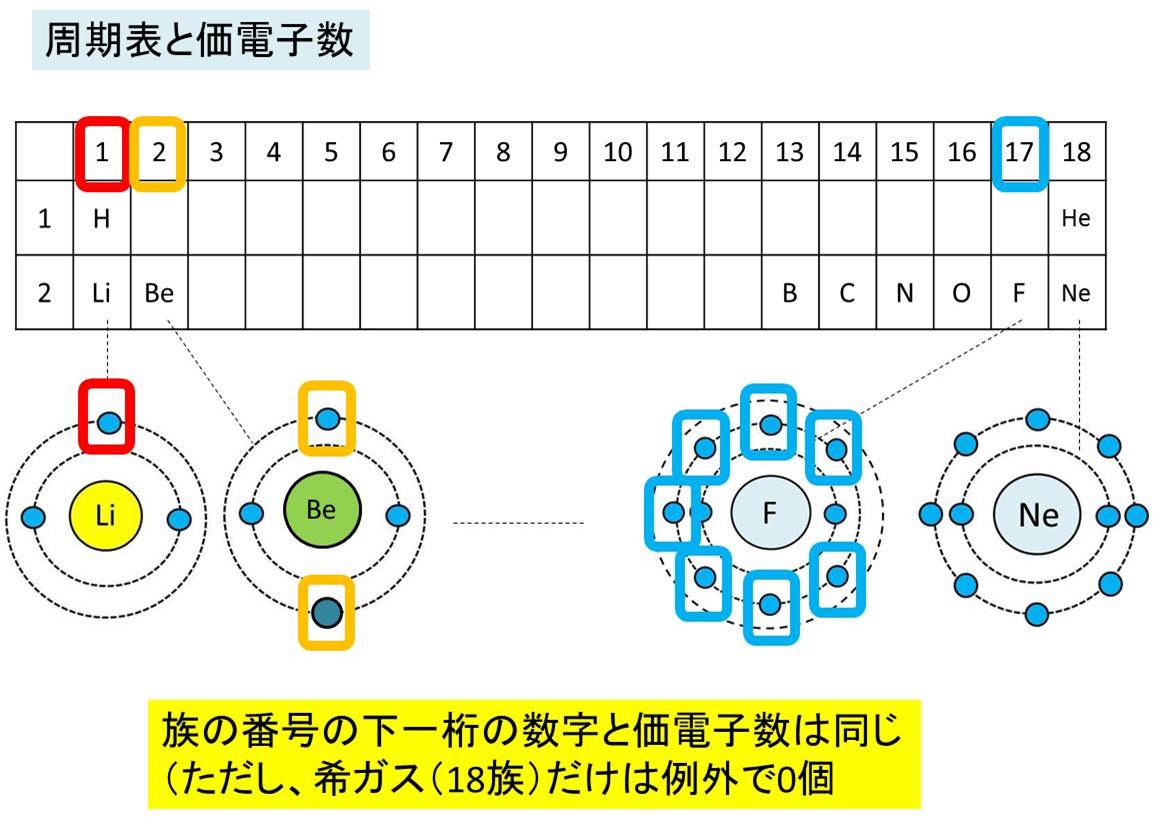
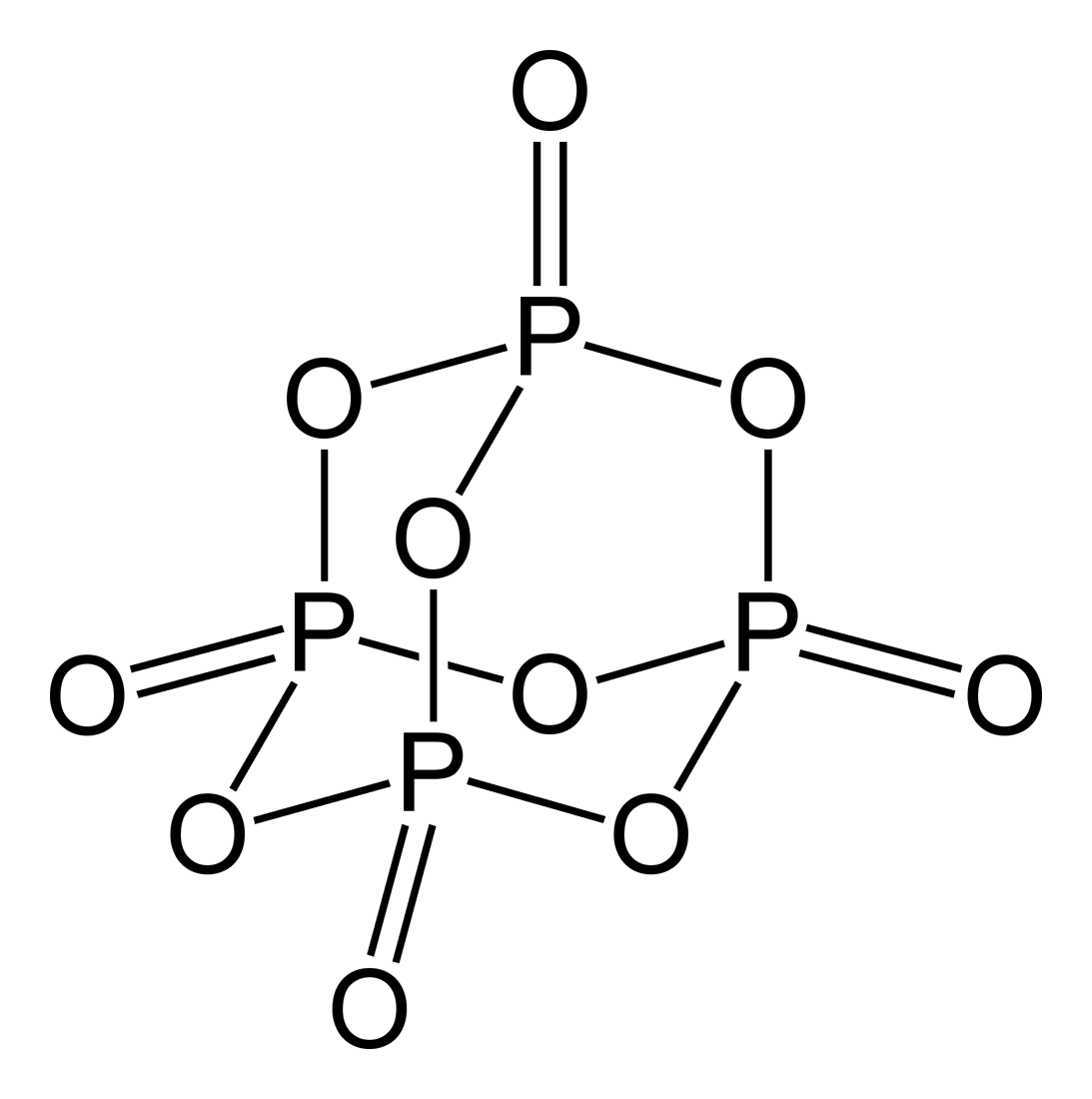
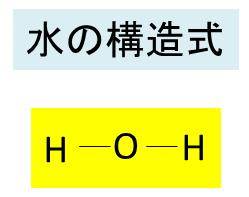
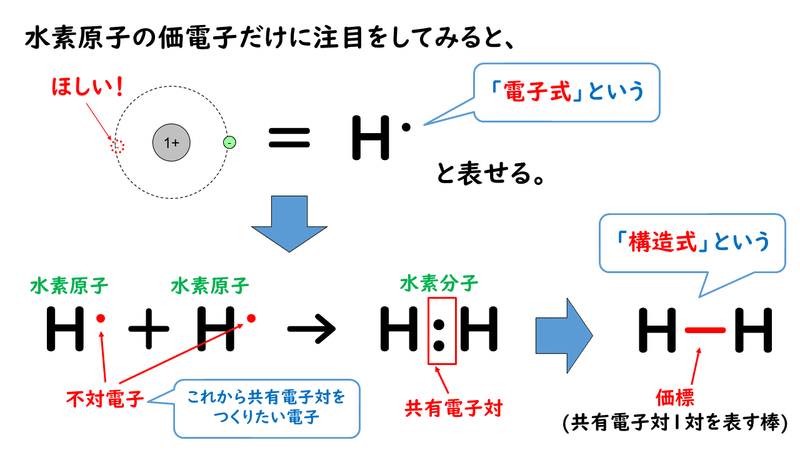
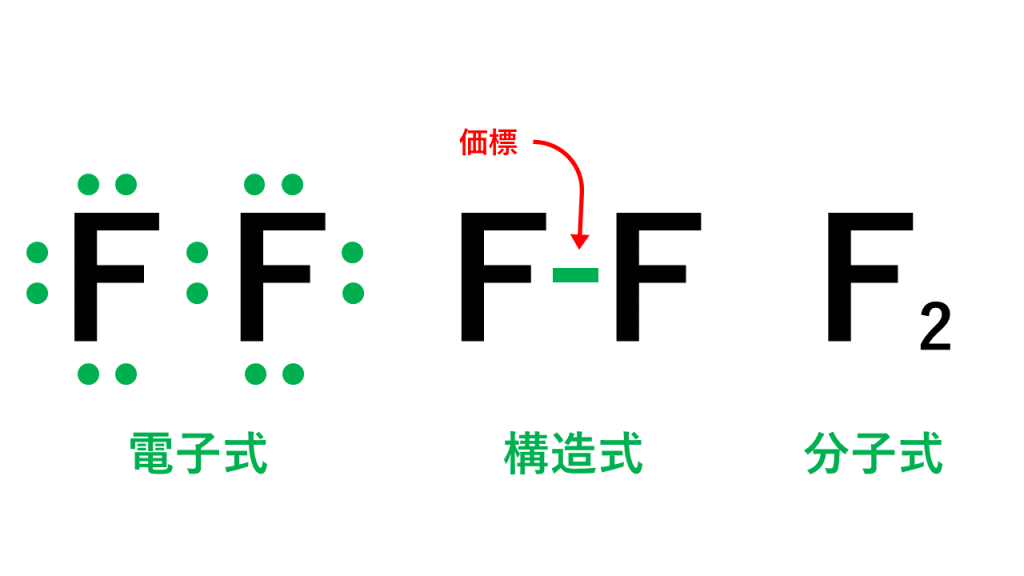
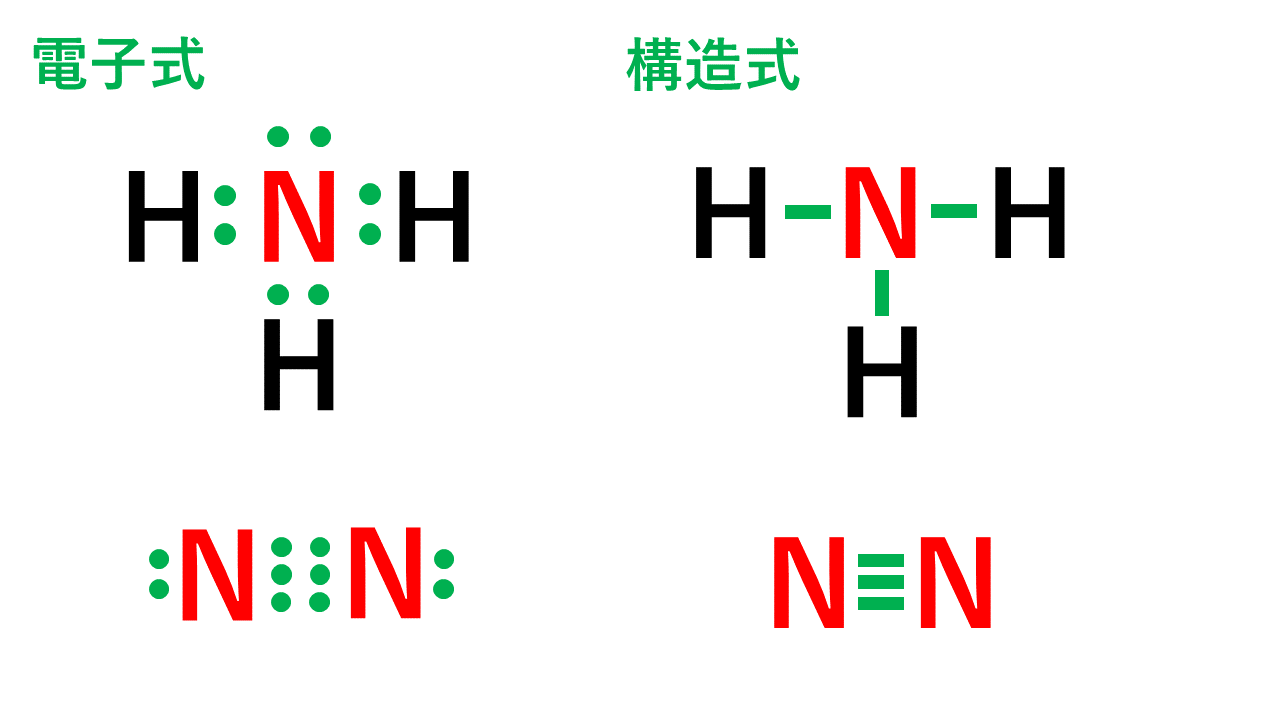
· 原子価とは、注目した原子から出ている価標(棒線)の本数のことです。 では、価標とは何だったのか、価電子や不対電子などとの違いについて説明していきます。 価電子数と原子価の違い 価電子とは最外殻に存在する電子の数のことです。価標 価標 (かひょう、bond)とは、 化合物 の 化学構造 を示す際に、 原子 間の 結合 を示すために用いる表示のことである。 五酸化二リン (十酸化四リン)の構造式。 この場合、 酸素 と リン の間をつなぐ線が価標である。分子を表す際、共有電子対を価標という線(-)で示した化学式を構造式という。 10.原子価 構造式において、それぞれの原子から出る価標の数を原子価という。原子価は、その原子がもつ不対電子の数に相当する。 例えば、水素分子h2の構造式はhhと表され、水素原子hの原子価は1価となる
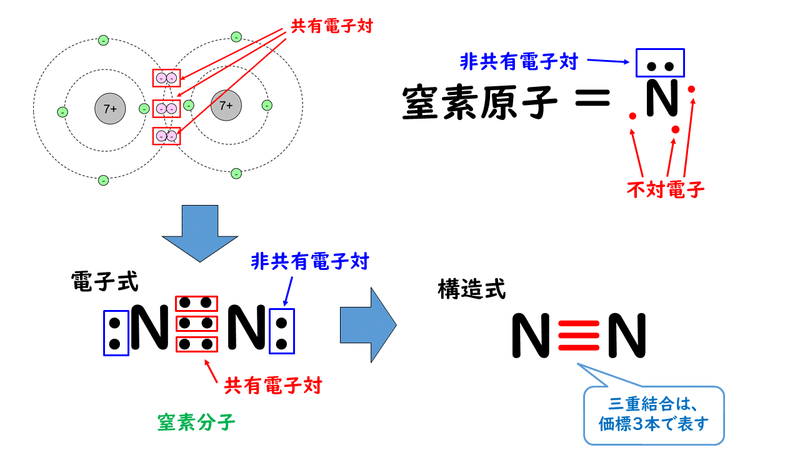
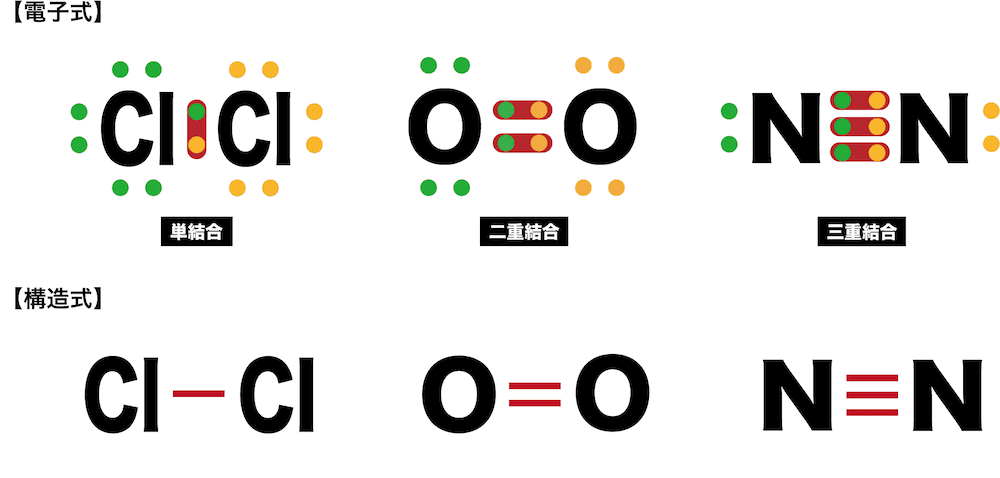
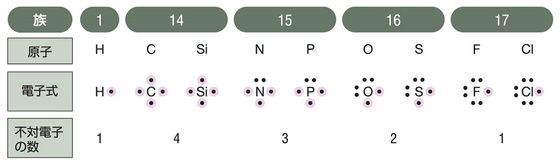
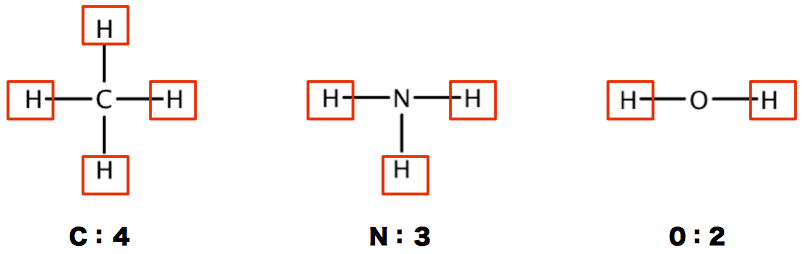
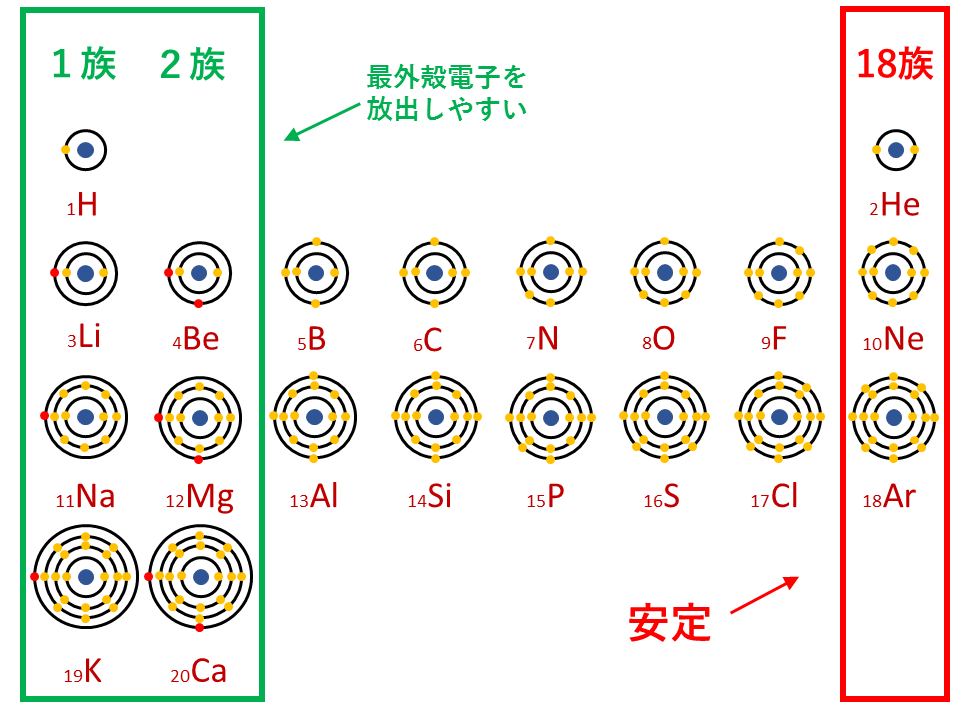
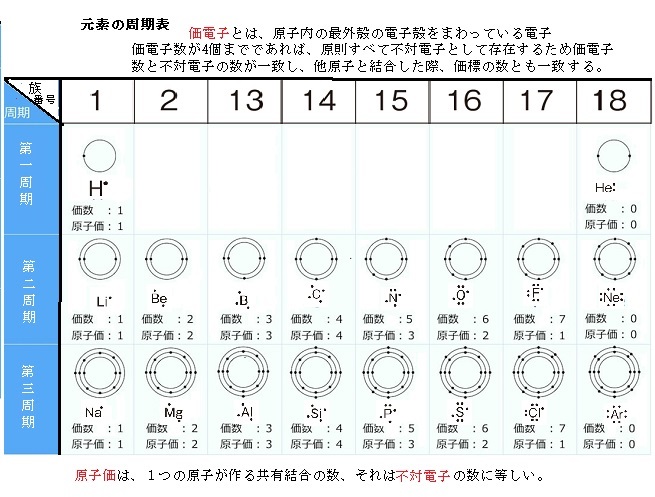
窒素原子nからは、価標(棒線)が3本出ている。窒素分子n 2 の場合も、三重結合となり、同様に窒素原子nからは、価標(棒線)が3本出ている。 よって、nの原子価は3、価電子数5とは一致しない。 目次へ 3)元素の周期律の意味精選版 日本国語大辞典 構造式の用語解説 〘名〙 化学式の一つ。分子内の原子相互の結合状態を図式的に表記した式。結合している各原子の元素記号を、単結合、二重結合、三重結合に応じて、それぞれ一本、二本、三本の短い線(価標)でつないで表わす。価標とはわかりやすく言えば、構造式書くときの手の本数です。 炭素なら4本、酸素なら2本なんでそれぞれ価標は4と2です。 分子の形は高校では完全丸暗記です。 説明できません。 興味あるなら大学で無機化学を勉強してください。 配位子とは例えば銅にアンモニア分子が配位結合する錯
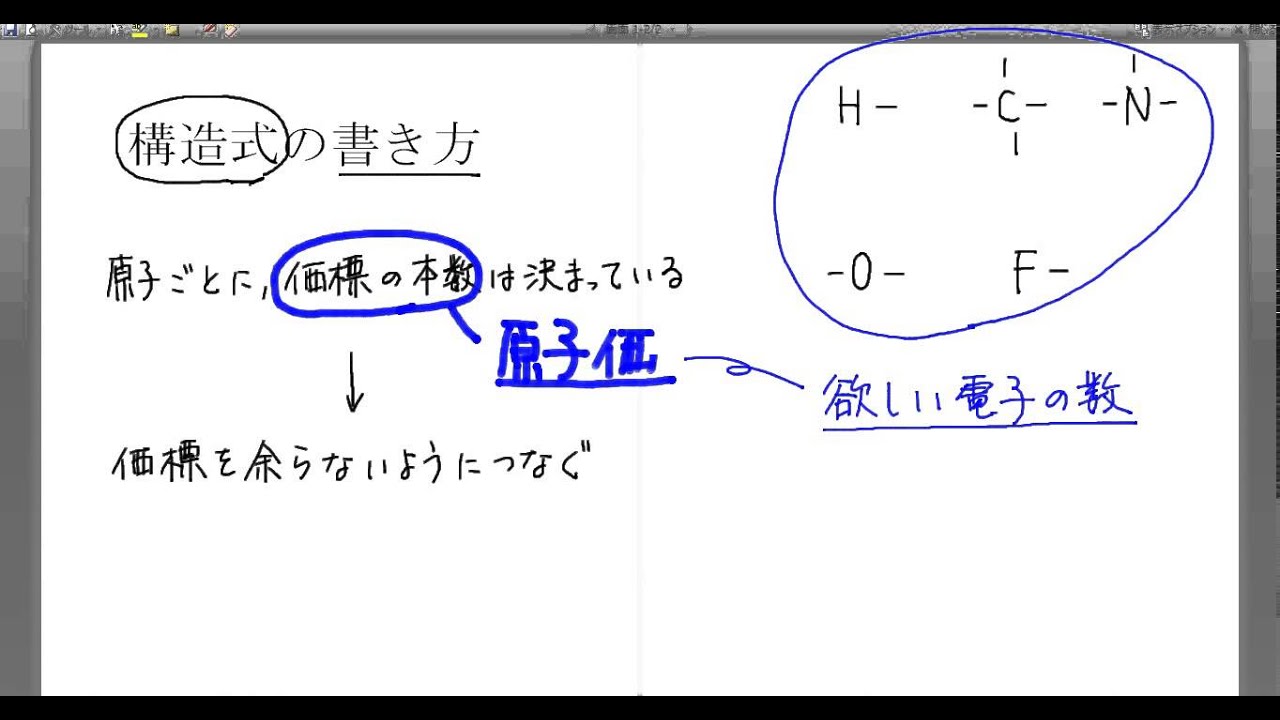
· アセチレンはH~C~C~Hが直線上に並んでいるので、右の形ですと減点対象になるかもしれません。 ※~は順番のみを示すために使用していますのでたいした意味はありません。 エチレンの模範解答が、その上の形ですから不正解とはならないと思います。 将来的にはフィッシャー投影式と呼ばれる厳密なルールに基づいた書き方もありますが、この段階では構造式:( 価標 )で原子のつながりを表す式 示性式:( 官能基 )を抜き出して示した式 分子式:原子の種類と個数を表した式。( c )、( h )の順に原子記号を並べる。これ以外は( アルファベット )順 に並べる。 ※ 構造式で分子の( 構造 )がわかる。示性式で( 官 · hiho (ハイホー) インターネットサービスプロバイダー トップページ│hiho hihoでんわCの設定変更について 「IPv6 インターネット(IPv6 PPPoE)接続」提供開始のお知らせ 「モバイルサービス」「携帯電話専用コース」サービス終了の




車山高原レア メモリーが語る 元素の周期表




価標 原子価 価電子の違いは
· https//detailchiebukuroyahoocojp/qa/question_detail/q uu8******** uu8********さん 1351(編集あり) 価電子の数ではなく、価電子の中の不対電子の数です。 原子どうしが共有結合するとき、不対電子1個ずつ出し合って結合し、これを1本の線で示したのが価標です。 ハロゲン原子は不対電子は1個です。 Cl₂の構造式はCl-Clです。 酸素原子は不対カクダイ 総合カタログ 2122 KAKUDAI pages list①構造式・示性式が、縦や斜めの位置に価標が無く横一列で描かれている場合は、次のような価標記号を使って点字化する。 単結合 4の点 二重結合 45の点 三重結合 456の点 単結合 2つ 46の点 なお、構造式や示性式の書き方の基本は化学式と同じ。




電子式 イオン式から配位結合 錯イオンの仕組みまでわかりやすく解説




官能基の単元についていくつか質問です 1 添付した写真のように 全 化学 教えて Goo
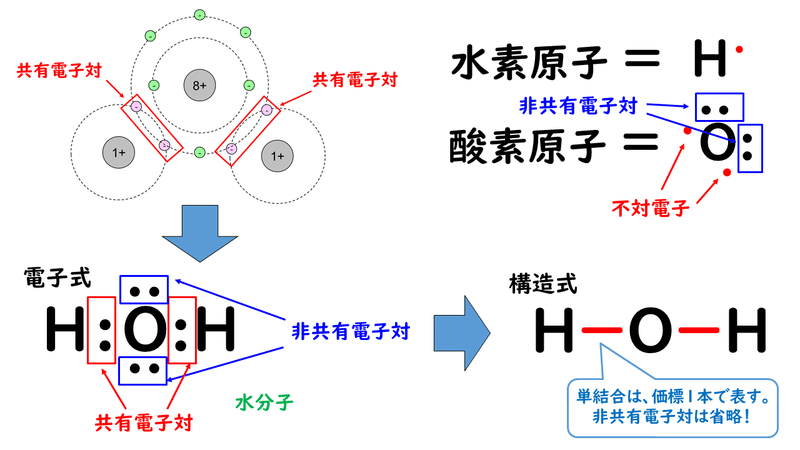
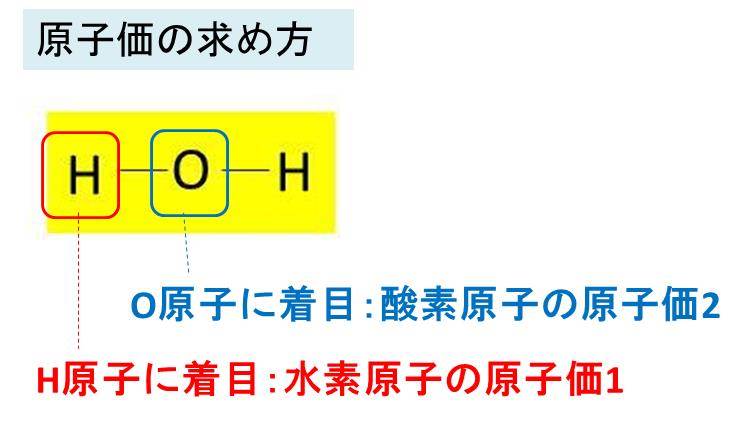
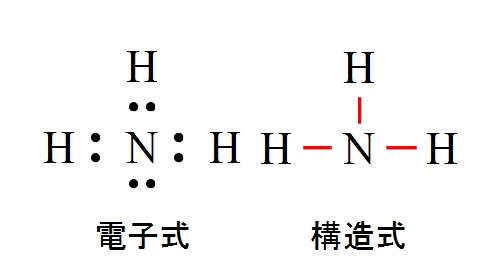
· この線のことを価標といいます!そして価標の数のことを原子価といいます! この場合では、水素の原子価は1、酸素の原子価は2ということになります! ところで、この原子価は電子式で水分子について考えた時にどこかで出てきた数字です。さてどこで出てきたのでしょうか。合(価標)の数だけ接着する。分子の形を考慮し ながら,マジックテープを2枚取り付けるとき (酸素の粒子モデルなど)は近づけて結合面が同 じ側にくるように粒子モデルに接着する。ま た,マジックテープを4枚接着するとき(炭素第一章 解説 Summary S11 分子式、示性式、構造式 分子式 : 1分子中に含まれる原子の種類と数を示す。;




明日期末試験です 至急教えてください Clear



受験基礎化学 11 共有結合 共有結合結晶 みかみの参考書ブログ
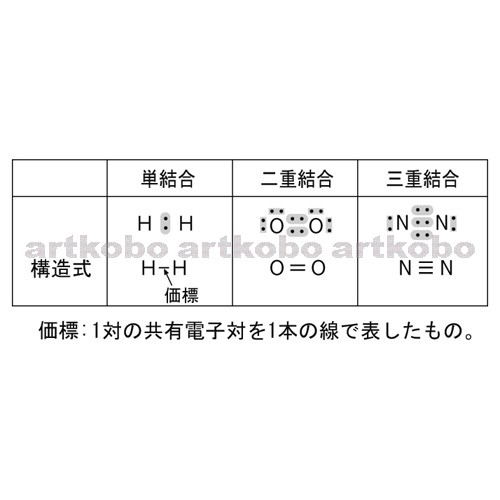
10^ {9}\leq 2^ {30} < 2\cdot 10^9 109 ≤ 230 < 2⋅ 109 つまり最高位の数は 1 1 1 である。 解答2 これくらいの計算は突破できる気合いが欲しい。 2 30 = 102 4 3 = 2^ {30}=1024^3= 230 = = なので最高位の数は 1 · 価標 * (英語bondは「結合」の意味で使われる) 現状高校でほぼ例外なく使われる。教科書の1冊だけが,本文には「1本の線」と書き,脚注に「価標」を紹介している。提案特別な呼称をつけない(必要なら「線」,「結合」などと呼ぶ。「1個の原子から出る価標の数」は,「1個の原子がつくる結合の数」でよい)。合を, 2本の価標 "="で二重 ?



Web教材イラスト図版工房 R Ch 物質の基本構成 29




高校化学 構造式 映像授業のtry It トライイット
株式会社ニッケンハードウエア 産業用部品 主に鋼製家具に使用する錠前、ハンドル、樹脂パーツ等 LED照明 事務所用、工場用、看板用、屋外用など事業所向けのLED照明 出入管理システム 事務所、マンションのエントランスの出入を管理する非接触IC · 原子価と価標・不対電子の関係 原子価は通常、 その原子がもつ価標及び不対電子の数と等しい。 ※原子価と価標・不対電子の数について詳しくは保存版最外殻電子・不対電子・原子価・価標の数一覧を参照 · まとめてざっくりいうと 価標とは、共有電子対を線で示したもののことであり、 原子価とは、ある原子がもつ不対電子の数のことです。 ちなみに同じ原子の場合、 価標の数=原子価です。



3 2 分子 おのれー Note



3
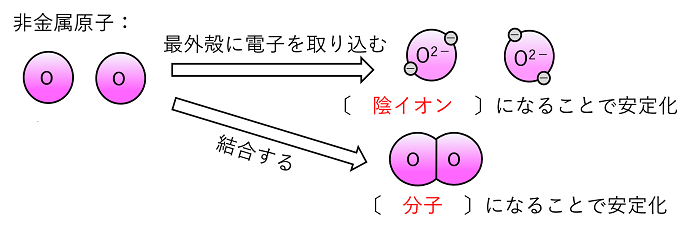
平成30年分 財産評価基準書 大東市 索引図|国税庁 現在のページ: トップページ > 平成30年分 > 大阪府 > 路線価図 > 大東市 (町丁名索引) > 大東市 (索引図)0:力価標定時の力価 α:滴定液の体膨張係数 (2プロパノール=106×103) t :試料滴定時の温度(℃) t 0 :力価標定時の温度(℃) 滴定曲線例 ※装置のオプション構成によっては、測定できない場合があります。 ④ 測定時の二酸化炭素の影響 酸価の測定は、水酸化カリウム標準液による滴定の&o 1 2 2 & &o &o 1 1 2 & 2 2 分子と共有結合 共有結合 非金属元素どうしの結合。 原子間で不足分の電子を出し合って共有することによってできる結合。



高校化学解説講義 共有結合 講義3 Youtube




で なぜ Fや Pや Siは含まれないのですか Clear
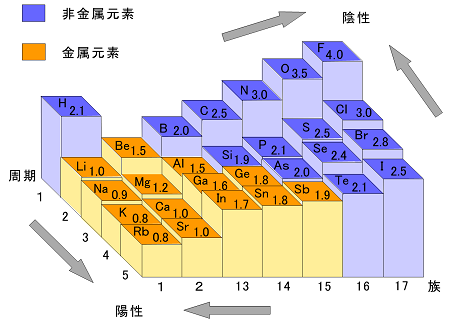
で三重結合を示す。たとえばぱ, 分子は, n三n と表される。 ん決まった立体的な構造をしてい 造を示しておらず, 水であれば きて 7 las 0 回答 おうす 約2年前 写真のようになるので、価電子5個を全て結合してしまうとN原子1つあたりの電子が12個になり、不安定3 分子の極性と分子間にはたらく力h 電気陰性度 共有結合している 2 種類の原子の間に存在する共有電子対は,どちらか一方の原子にかたよって存在している場合が多い。 このように,共有電子対がかたよって存在するのは,共有電子対を引き付ける強さが原子によって異なるからである。力価標定時と試料測定時の 液温が異なる場合には、力価補正を行う必要があります(力価補正の詳細は、アプリケーションデ ータb19 を参照ください) キーワード:医薬品、日本薬局方、過塩素酸滴定、力価標定、非水滴定、フタル酸水素カリウム 滴定曲線例




化学基礎 物質の構成34 構造式と原子価 9分 Youtube




高校化学 構造式 映像授業のtry It トライイット
ビブリオバトルとは ― どこでも手軽に楽しめる書評ゲームです。 07年、京都大学大学院の大学院生だった 谷口忠大さん(現立命館大学理工学部教授)が、輪読会で読む本は自分たちで決めようと考案しました。 「人を通して本を知る、本を通して人 · 問題はセンター試験レベルではほとんどないと思いますが 正しく用語を使えるようになるために意識して使い分けましょう。 さてさて、分子を構造式で表示するとき、 1組の共有電子対による共有結合(単結合)を1本の線で表します。 この線を「価標」といいます。 2組の共有電子対による共有結合(二重結合)なら2本、 3組の共有電子対による共有結合カールフィッシャー試薬の力価標定で測定した結果について、カールフィッシャー試薬 の力価を算出する(6)。 カールフィッシャー試薬の力価(mg H2O/mL)=S_H2O /V S_H2O:滴定に用いた力価標定用試薬の含水量(mg) V:滴定に要したカールフィッシャー試薬量(mL) 食用植物油脂の水分



受験基礎化学 11 共有結合 共有結合結晶 みかみの参考書ブログ
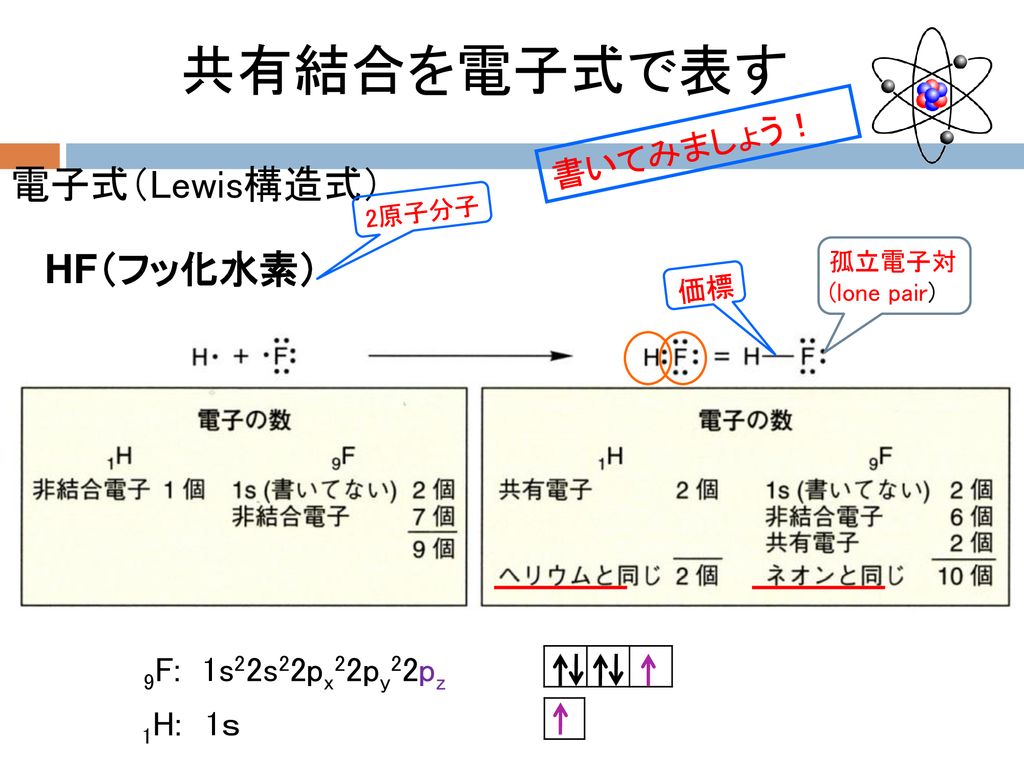



教養の化学 第8週 13年11月11日 担当 杉本昭子 Ppt Download
か‐ひょう〔‐ヘウ〕価標 化合物 の 化学構造 を示すのに用いる、 原子 間の 結合 を示す表示。 単結合 を1本、 二重結合 を2本、 三重結合 を3本の 線 などで表す。




価標 原子価 価電子の違いは
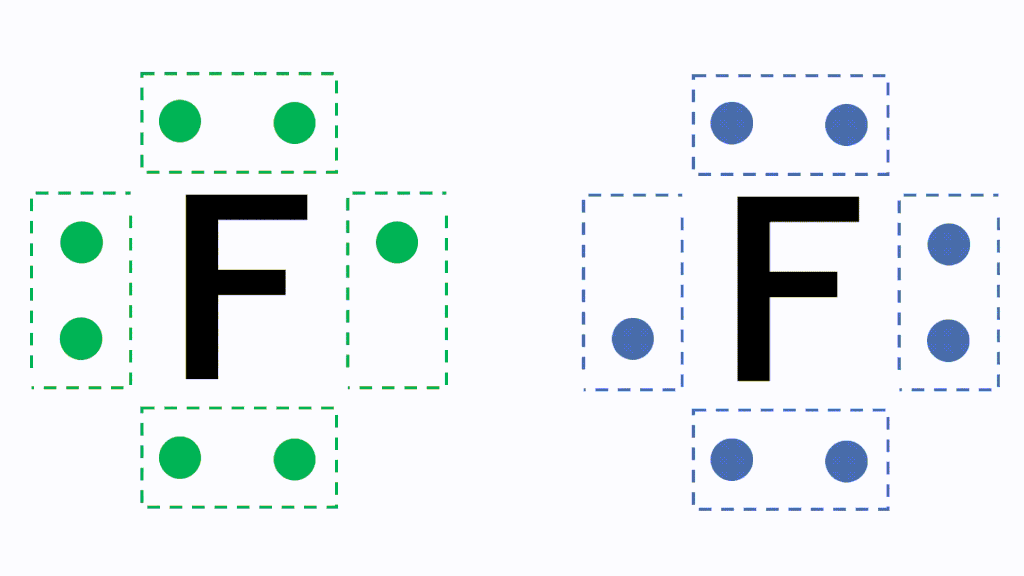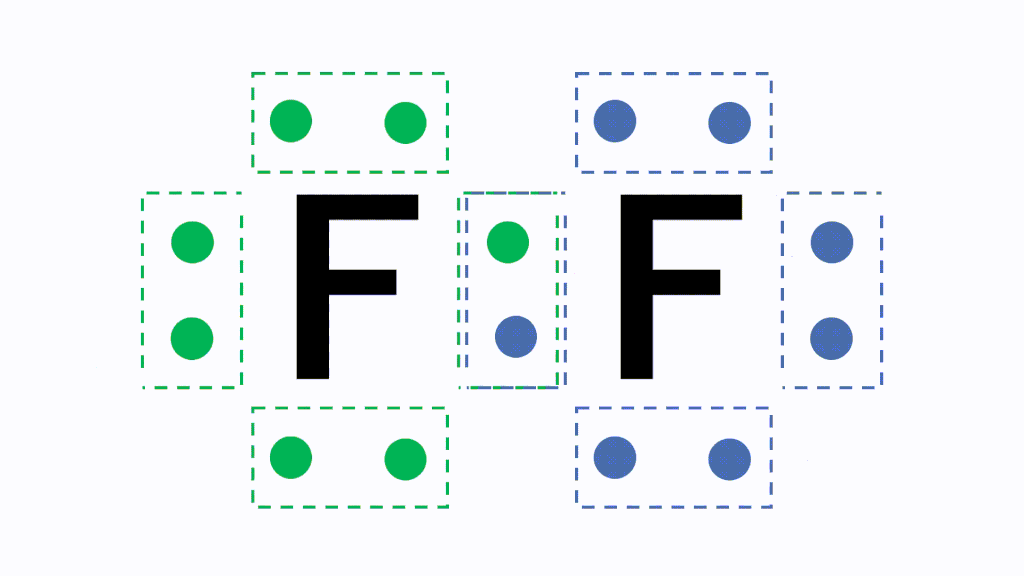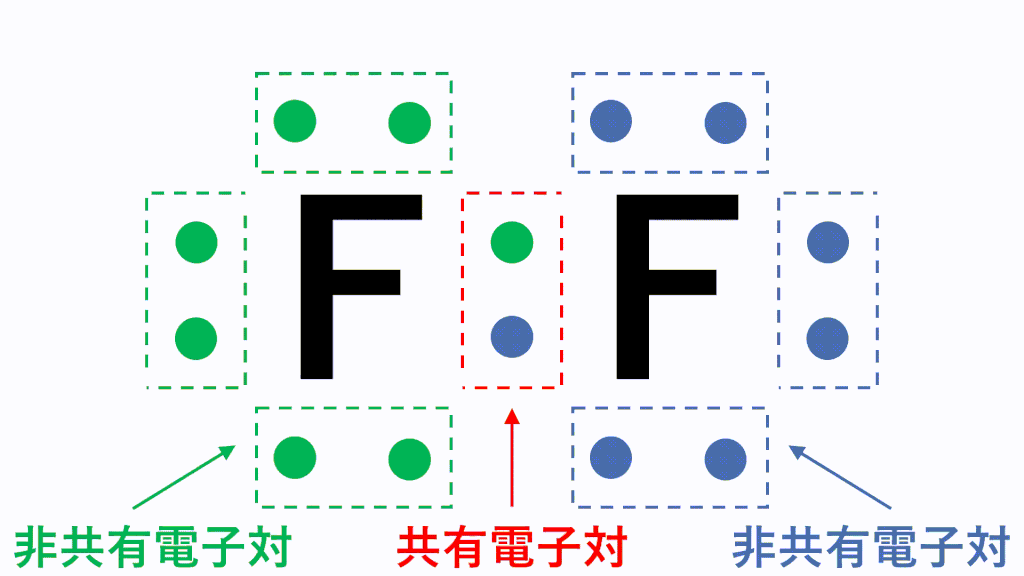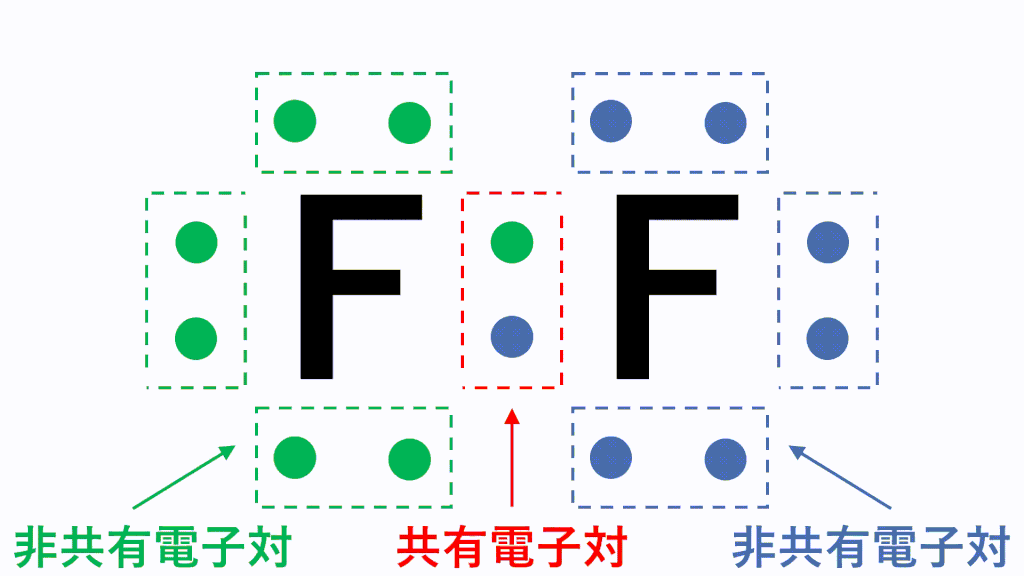



5分でわかる 原子価の意味と一覧 価電子 価標の違い を図で徹底解説 サイエンスストック 高校化学をアニメーションで理解する



5分でわかる 原子価の意味と一覧 価電子 価標の違い を図で徹底解説 サイエンスストック 高校化学をアニメーションで理解する




教えてください Clear




原子価とは価電子とは違うのでしょうか 今回の場合なぜ2価と分かるのか教えてください Clear




原子価とは 原子価の求め方までわかりやすく解説 高校生向け受験応援メディア 受験のミカタ



Www Pen Kanagawa Ed Jp Y Meiho H Oshirase Documents 2 Kagakukiso 0619 Pdf




メルカリ 化学基礎の教科書 参考書 399 中古や未使用のフリマ



3 2 分子 おのれー Note



Q Tbn And9gct2kjzflwnhsaxoolbww0wtjjkb 0ntuszb Atdhungylgoed 5 Usqp Cau



Http Mi224awk Starfree Jp Download Chemformbook W Pdf




精油の化学 基材 Hir0 Tのブログ




高校化学基礎 原子価とは 映像授業のtry It トライイット




分子と共有結合



共有結合 例 イオン結合や配位結合との違いなど 化学のグルメ



分子と共有結合



3 2 分子 おのれー Note



受験基礎化学 11 共有結合 共有結合結晶 みかみの参考書ブログ



分子と共有結合




電子式 イオン式から配位結合 錯イオンの仕組みまでわかりやすく解説




原子価の意味と一覧 価電子 価標の違い Vicolla Magazine




原子価の意味と一覧 価電子 価標の違い Vicolla Magazine



車山高原レア メモリーが語る 元素の周期表



不対電子の数や 価標の数 価数 はわかるのですが 原子価がよく理解できません Yahoo 知恵袋




化学 構造式 オンライン無料塾 ターンナップ




原子価とは 原子価の求め方までわかりやすく解説 高校生向け受験応援メディア 受験のミカタ
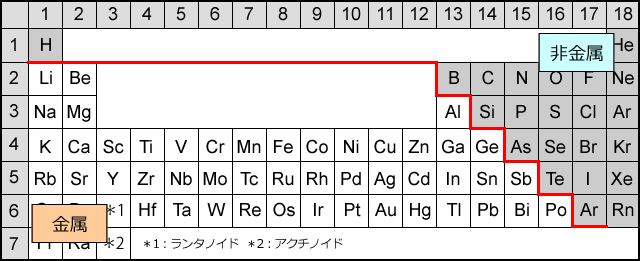



第6回 金属と非金属 化学結合 1 共有結合 私立 国公立大学医学部に入ろう ドットコム



Www Pen Kanagawa Ed Jp Y Meiho H Oshirase Documents 2 Kagakukiso 0619 Pdf




原子価とは 原子価の求め方までわかりやすく解説 高校生向け受験応援メディア 受験のミカタ




分子と共有結合




1 2 1 H H Ci H 0 H Descubre Como Resolverlo En Qanda



化学の 原子価 と 価標 って一体どういうものなんですか わかりや Yahoo 知恵袋



この示性式はあっていますか 示性式 官能基とそれ以外に分けた式 と構 Yahoo 知恵袋
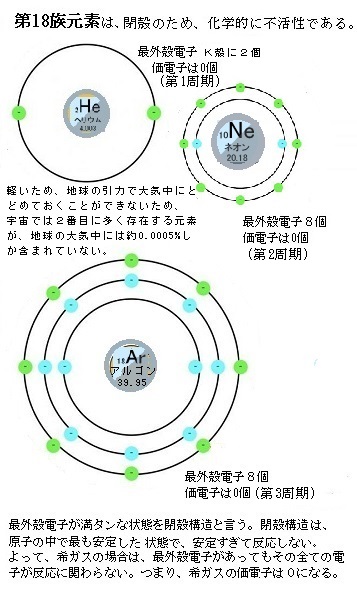



車山高原レア メモリーが語る 元素の周期表




Lihat Cara Penyelesaian Di Qanda
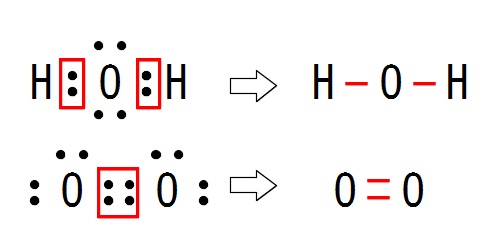



共有結合の種類と構造式の書き方




高校有機化学 有機化合物の表現 構造式 示性式 分子式 組成式 と代表的な官能基まとめ 受験の月
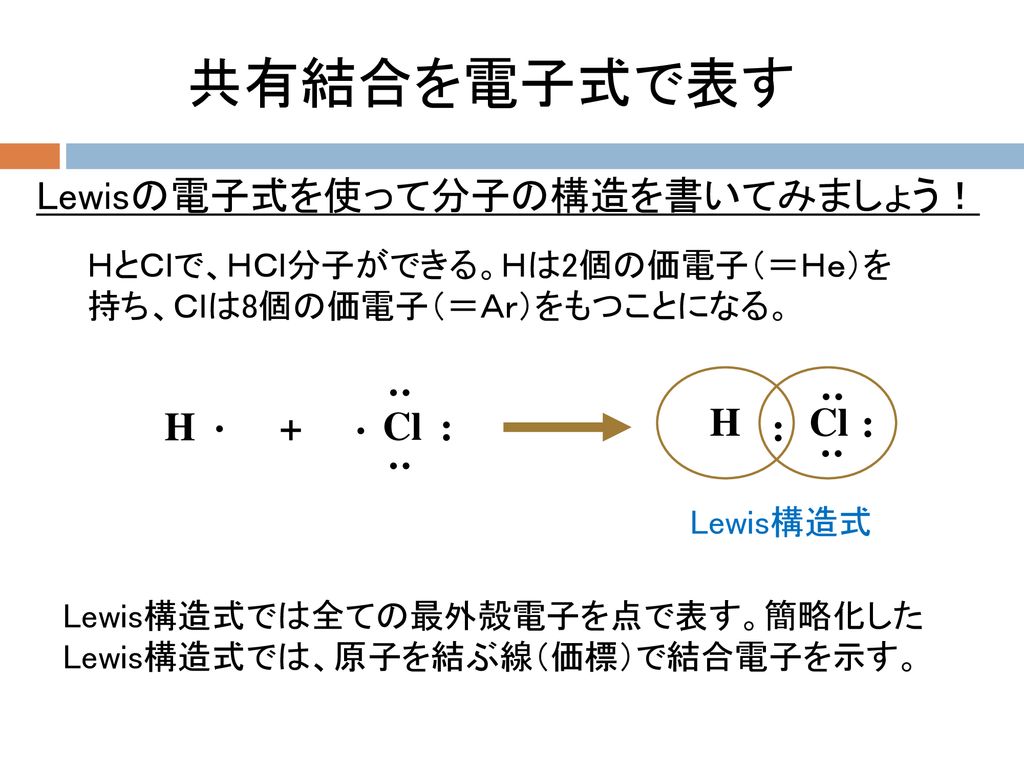



教養の化学 第8週 13年11月11日 担当 杉本昭子 Ppt Download



科学 化学 Pararinpoppin In Hell




1つの原子から出ている価標の数 とはどういう意味でしょうか 価標の意味が分かりま Clear




価標の意味 用法を知る Astamuse




原子価とは 原子価の求め方までわかりやすく解説 高校生向け受験応援メディア 受験のミカタ



価標 原子価 価電子の違いは




共有結合とは 例 結晶 イオン結合との違い 半径 理系ラボ




原子価とは 原子価の求め方までわかりやすく解説 高校生向け受験応援メディア 受験のミカタ



Q A



価標 Wikipedia



価標 原子価 価電子の違いは



示性式は価標を書かないはずなのに何故ここでは示性式に価標が書かれているので Yahoo 知恵袋




なんでn2の構造式は価標が3つだけなんですか 価電子が5つあって写真の右下のように全 Clear




共有結合の種類と分子の形と結晶



原子価 一覧 価標 不対電子との関係など 化学のグルメ



Www Pen Kanagawa Ed Jp Y Meiho H Oshirase Documents 2 Kagakukiso 0619 Pdf



3 の結合手というのは単結合をしてる訳では無いので価標とは別物でし Yahoo 知恵袋



糖の構造式を書くとき手前の価標を太くする必要はありますか 試験で Yahoo 知恵袋



価標 原子価 価電子の違いは



原子価の意味と一覧 価電子 価標の違い Vicolla Magazine



Www Toshin Com Exams Files Upload Review Tool 7 24 4 1 Pdf



3 2 分子 おのれー Note



電子式の書き方と一覧 構造式と分子式の違い Vicolla Magazine



混成軌道



5分でわかる 原子価の意味と一覧 価電子 価標の違い を図で徹底解説 サイエンスストック 高校化学をアニメーションで理解する



Www Pen Kanagawa Ed Jp Y Meiho H Oshirase Documents 2 Kagakukiso 0619 Pdf



車山高原レア メモリーが語る 元素の周期表



5分でわかる 原子価の意味と一覧 価電子 価標の違い を図で徹底解説 サイエンスストック 高校化学をアニメーションで理解する



原子価の意味と一覧 価電子 価標の違い Vicolla Magazine




Image Taigapotetomeat Flickr




共有結合と分子




電子式 構造式 Chemihack おうちで学べる化学




高校化学基礎 電子式 二重結合 構造式 Youtube




構造式の書き方 化学の基本として知っておきたいルールとは 高校生向け受験応援メディア 受験のミカタ



1



Q Tbn And9gcqsu2jb Tdmwzj3zo15vre8xnlcrg8w6bx73rtfw5jpfmdtqdct Usqp Cau




教養の化学 第10週 13年12月2日 担当 杉本昭子 Ppt Download




1 2 1 H H Ci H 0 H Descubre Como Resolverlo En Qanda




価標と原子価の違いって 受験に化学を必要とする人へ




1つの原子から出ている価標の数 とはどういう意味でしょうか 価標の意味が分かりま Clear




5分でわかる 原子価の意味と一覧 価電子 価標の違い を図で徹底解説 サイエンスストック 高校化学をアニメーションで理解する




原子価とはなんでしょうか Clear



共有結合の種類と分子の形と結晶



分子の極性と分子間にはたらく力



問題文に 構造式を書く時には 水素原子との結合を表す価標は省略し Yahoo 知恵袋



車山高原レア メモリーが語る 元素の周期表
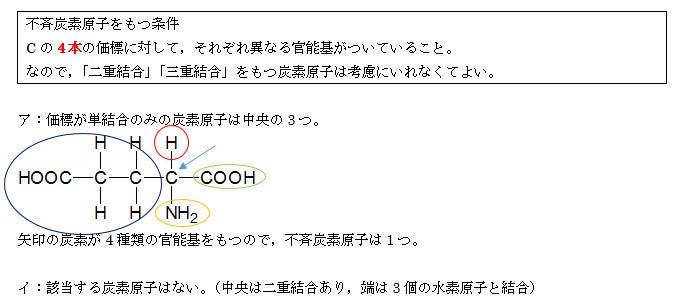



02 第5問 問2 不斉炭素原子の個数 化学がちょっとだけ好きな社労士




18 二重結合 高校化学の浮き輪 文系脳を救助する Youtube



化学の 原子価 と 価標 って一体どういうものなんですか わかりや Yahoo 知恵袋




1つの原子から出ている価標の数 とはどういう意味でしょうか 価標の意味が分かりま Clear
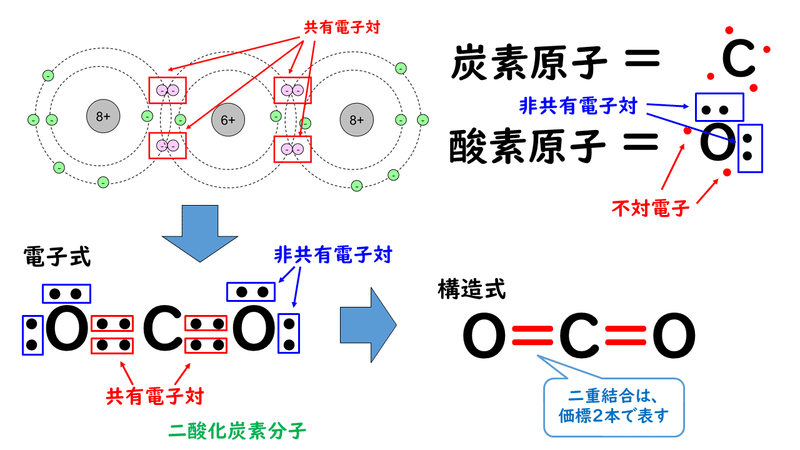



3 2 分子 おのれー Note


コメント
コメントを投稿